2020年8月14日,复宏汉霖(2696.HK)宣布,其自主开发和生产的曲妥珠单抗汉曲优®(HLX02,欧盟商品名:Zercepac®)正式获国家药品监督管理局(National Medical Products Administration, NMPA)批准上市。
此前在2020年7月27日,曲妥珠单抗HLX02(欧盟商品名:Zercepac®)获欧盟委员会(European Commission,EC)批准上市登陆欧洲市场。可在全部欧盟成员国以及欧洲经济区国家挪威、冰岛和列支敦士登上市销售,其首个欧盟订单产品已运抵复宏汉霖商业合作伙伴Accord于英国的生产基地,未来在欧洲的商业化将由Accord负责。

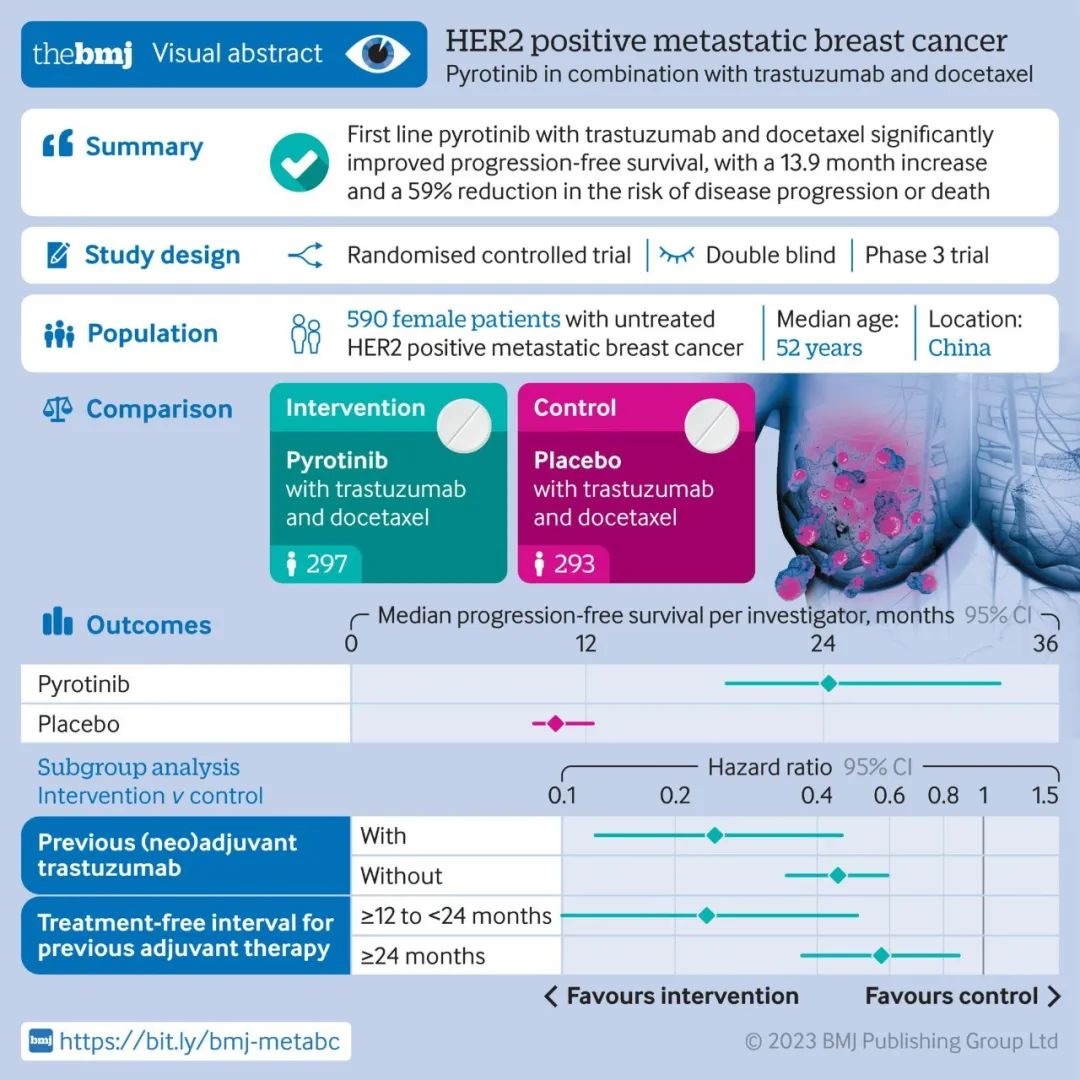
本品为首个中欧双批的国产单抗生物类似药。汉曲优®通用名为注射用曲妥珠单抗(规格150mg/瓶,不含防腐剂),获得原研在中国已获批准的所有适应症:1)HER2阳性早期乳腺癌;2)HER2阳性转移性乳腺癌;3)HER2阳性转移性胃癌。
曲妥珠单抗已于2017年被纳入中国国家医保目录,根据国家医疗保障局发布的《基本医疗保险用药管理暂行办法》,《基本医疗保险药品目录》(以下简称《药品目录》)实行通用名管理,《药品目录》内药品的同通用名药品自动属于基本医疗保险基金支付范围。根据IQVIA数据统计,2018年、2019年曲妥珠单抗于中国境内销售金额分别约为27.3亿和45.7亿人民币。
复宏汉霖HLX02(注射用曲妥珠单抗)中国研发历程
2015年7月及2016年1月,HLX02用于乳腺癌、胃癌的适应症先后获得原国家食品药品监督管理总局(CFDA)临床试验批准。
2018年9月,第21届全国临床肿瘤学会(CSCO)年会期间,以中国市售原研曲妥珠单抗、欧洲市售原研曲妥珠单抗为对照的HLX02 1期临床试验数据首次公布。结果显示,HLX02与原研曲妥珠单抗具有相似的药代动力学特征、安全性、耐受性和免疫原性,该数据也同样亮相于2018年ESMO Asia。
2019年4月,HLX02正式获国家药品监督管理局(NMPA)新药上市申请受理,之后被纳入优先审评程序。
2020年8月14日,正式获批上市。

【商品名】汉曲优
【通用名】注射用曲妥珠单抗
【规格】150mg/瓶
药融圈数据获悉,8月24日中国开卖
本品每瓶价格为1688元